Détail du poste
Job Description Summary
Le rôle du/de la Clinical Project Manager (CPM) est de soutenir le développement clinique de nouveaux agents d'imagerie conformément aux lignes directrices ICH-GCP et aux Procédures Opérationnelles Standard (SOP).Le/La CPM agit en tant que Study Manager pour les essais cliniques de grande envergure, globaux et/ou complexes qui lui sont confiés. Il/Elle fournit à l'équipe projet une direction globale, des attentes claires en matière de livrables ainsi que le leadership nécessaire à la gestion, à la conduite et à l'achèvement réussis d'un programme d'essais cliniques.
Le/La CPM planifie, met en oeuvre et pilote l'ensemble des activités des essais cliniques conformément au Plan Global de Développement Clinique (Clinical Development Plan - CDP), aux plans de programme produit, et dans le respect des Bonnes Pratiques Cliniques (GCP), des Procédures Opérationnelles Standard (SOP), des politiques de l'entreprise, des lignes directrices et des standards internes.
**
The role of the Clinical Project Director (CPD) is to support the clinical development of new imaging agents in accordance with ICH-GCP and Standard Operating Procedures (SOPs).
The CPD acts as the Study Manager for assigned large, global and/or complex Clinical studies and provides the study team with overall direction, clear expectations for deliverables and the leadership necessary for the successful management, conduct and completion of a clinical study program. To plan, implement and drive all aspects of clinical studies according to the Global Clinical Development Plan (CDP), Product Program Plans and in compliance with Good Clinical Practice (GCP), Standard Operating Procedures (SOP), Corporate Policies, Guidelines and internal Standards.
Job Description
Domaines de responsabilité et missions
Garantir que les activités et jalons des études sont planifiés, validés et atteints conformément au plan global de développement clinique (CDP, le cas échéant), ainsi qu'aux plans de jalons et de recrutement associés.
Évaluer la faisabilité des essais cliniques en collaboration avec les autres fonctions concernées.
Assurer la préparation, dans les délais et avec un niveau de qualité approprié, de la documentation des études (protocoles, amendements, cahiers d'observation / eCRF, plans d'étude, rapports d'étude), en collaboration avec les fonctions internes et les CRO, le cas échéant.
Veiller à l'obtention des soumissions réglementaires et des approbations des autorités compétentes et comités d'éthique.
Garantir que la déclaration des événements indésirables (graves) ((S)AE) est réalisée conformément aux exigences internes et réglementaires.
Apporter son expertise aux spécifications d'externalisation clinique et aux activités d'achats afin de contribuer à la préparation des dossiers d'appel d'offres (RFP) et à la sélection des prestataires et CRO.
Participer à la sélection des prestataires de services, CRO et autres fournisseurs externes, en collaboration avec le département Sourcing, le Directeur des Alliances Stratégiques et l'équipe projet.
Sélectionner, superviser et gérer activement les prestataires, consultants et fournisseurs externes impliqués dans l'étude clinique (par exemple : laboratoire central, fournisseur EDC, CRO, fournisseur ECG).
Construire des relations solides afin de maximiser la performance et la valeur apportées par les prestataires.
Mettre en place une culture de responsabilité partagée afin de garantir la performance des fournisseurs.
Faciliter une résolution efficace, collaborative et proactive des problèmes et conflits avec les prestataires de services.
Assurer la formation des prestataires aux procédures opérationnelles standard (SOP) GE HealthCare applicables.
Réaliser les premiers contacts et participer à l'évaluation et à la sélection des investigateurs qualifiés pour les programmes cliniques.
Superviser la réalisation des visites de pré-sélection, d'initiation, de monitoring et de clôture des centres investigateurs.
Superviser la négociation et le suivi des budgets des sites conformément aux accords financiers établis.
Superviser le suivi des inclusions de sujets par centre et fournir, sur demande, des rapports d'activité clinique à la direction.
Garantir que les centres cliniques disposent de fournitures adéquates pour la bonne conduite des essais.
Encadrer, le cas échéant, le travail de Study Managers moins expérimentés.
Gérer le budget des études cliniques.
Participer aux réunions mensuelles de Recherche Clinique et présenter l'avancement des études dont il ou elle a la charge.
Contribuer aux activités de développement, de revue et d'harmonisation des processus globaux (SOP, lignes directrices, formulaires).
Identifier et communiquer les opportunités d'amélioration de l'infrastructure locale et globale de la Recherche Clinique chez GE HealthCare.
Piloter, en collaboration avec l'équipe projet, l'identification proactive, l'évaluation et la gestion des risques liés aux études cliniques.
Garantir que les opérations quotidiennes des études sont conformes au système qualité et aux exigences réglementaires, et maintenir un état permanent de préparation aux audits.
Identifier, en collaboration avec le Directeur Médical, les membres des comités d'étude (comité de pilotage, comité de publication, etc.), assurer la mise en place des contrats et chartes, et garantir leur suivi et pilotage dans la durée.
Participer aux réunions de revue des études avec les Autorités Compétentes et/ou les Comités d'Éthique, le cas échéant.
Qualifications
Diplôme scientifique avec une expérience significative et démontrée dans la gestion d'essais cliniques complexes de phases I à IV dans l'industrie de la santé.
Excellente connaissance de l'ensemble du processus des essais cliniques, incluant la planification, l'exécution, le reporting et la publication des résultats.
Compétences avérées en communication écrite et orale, à tous les niveaux de l'organisation.
Compétences et aptitudes
Excellentes compétences en communication écrite et orale, relations interpersonnelles solides et capacités de présentation.
Sens aigu de l'organisation et de la structuration, avec une forte attention au détail.
Capacité à travailler de manière autonome, méthodique et structurée.
Esprit d'équipe, diplomatie et capacité de coopération.
Capacité à prendre des décisions de manière efficace et pragmatique.
Capacité démontrée à gérer des études complexes et/ou multiples dans un environnement international.
Compétences en leadership reconnues.
Disponibilité pour se déplacer selon les besoins (réunions d'équipes projet, visites de sites, présentations clients, réunions ou conférences professionnelles).
Approche flexible et adaptable.
**
Areas of Responsibility & Tasks
Ensure that study activities and milestones are planned, agreed, and achieved in line with the overall clinical development plan (CDP, if applicable), as well as milestone and recruitment plans.
Determine the feasibility of running clinical studies in collaboration with relevant internal functions.
Ensure the timely and accurate preparation of study documentation, including protocols, amendments, CRFs/eCRFs, study plans, and study reports, in collaboration with internal teams and CROs as required.
Ensure that all Regulatory Authority and Ethics Committee submissions and approvals are obtained.
Ensure that (Serious) Adverse Event ((S)AE) reporting is performed in compliance with internal procedures and external regulatory requirements.
Provide clinical expertise to outsourcing specifications and purchasing activities to support RFP development and the selection of service providers and CROs.
Participate in the selection of service providers, CROs, and other external vendors in collaboration with Sourcing, Strategic Alliances, and the study team.
Select, supervise, and actively manage contractors, consultants, and external vendors involved in the clinical study (e.g. CROs, central labs, EDC vendors, ECG vendors).
Build strong relationships to maximize performance and value delivered by service providers
Foster a culture of joint accountability to ensure vendor performance
Facilitate efficient and collaborative resolution of issues and conflicts with service providers
Facilitate vendor training on applicable GE HealthCare SOPs.
Perform initial investigator contact and participate in the assessment and selection of qualified investigators for clinical programs.
Oversee pre-selection, initiation, monitoring, and closeout site visits.
Oversee negotiation and tracking of site budgets in line with financial agreements.
Oversee tracking of subject enrollment per site and provide management with clinical activity reports as requested.
Ensure that clinical trial sites have adequate supplies to conduct the study.
May supervise the work of less experienced study managers.
Manage the clinical study budget.
Attend monthly Clinical Research Meetings and report progress on assigned studies.
Participate in the development, review, and harmonization of SOPs, guidelines, and forms.
Identify and communicate opportunities for improvement within local and global Clinical Research infrastructure.
In collaboration with the project team, lead proactive identification, assessment, and management of clinical study risks.
Ensure that day-to-day clinical study operations comply with the Quality System and applicable regulations, maintaining continuous audit readiness.
In collaboration with the Medical Director, identify study committee members (e.g. steering committees, publication committees), ensure contracts and charters are in place, and provide ongoing oversight.
Attend Competent Authority and Ethics Committee study review meetings as required.
Qualifications
Degree in a science-related field with extensive proven experience in managing complex Phase I-IV clinical studies within the healthcare industry.
Excellent knowledge of all aspects of the clinical study process, including planning, execution, reporting, and publication of results.
Strong written and verbal communication skills, with the ability to interact effectively at all organizational levels.
Skills & Attributes
Excellent written and oral communication skills, strong interpersonal skills, and good presentation abilities.
Highly organized and structured, with strong attention to detail.
Ability to work independently and in a systematic manner.
Diplomatic, cooperative, and effective team player.
Decisive and solution-oriented mindset.
Proven ability to manage complex studies and/or multiple studies across different regions.
Demonstrated leadership skills.
Willingness to travel as required for study team meetings, site visits, client presentations, and professional meetings or conferences.
Flexible and adaptable approach.
About Us
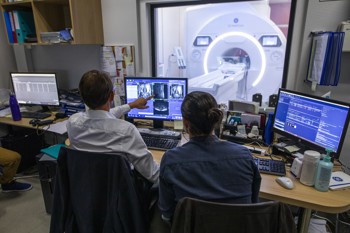
GE HealthCare is a leading global medical technology and digital solutions innovator with over 100 years of healthcare industry experience and around 50,000 employees globally. We enable clinicians to make faster, more informed decisions through intelligent devices, data analytics, applications and services, supported by our Edison intelligence platform. We operate at the center of an ecosystem working toward precision health - digitizing healthcare, helping drive productivity and improving outcomes for patients, providers, health systems and researchers around the world.
Our total rewards are designed to unlock your ambition by giving you the boost and flexibility you need to turn your ideas into world-changing realities. Our salary and benefits are everything you'd expect from an organization with global strength and scale, and you'll be surrounded by career opportunities in a culture that fosters care, collaboration and support.
GE HealthCare is an Equal Opportunity Employer where inclusion matters. Employment decisions are made without regard to race, color, religion, national or ethnic origin, sex, sexual orientation, gender identity or expression, age, disability, protected veteran status or other characteristics protected by law.
GE HealthCare - Creating a world where healthcare has no limits
#LI-CM1
Additional Information
Relocation Assistance Provided: No
Les étapes de recrutement
Les étapes de recrutement peuvent varier selon l'offre à laquelle vous postulez.
-
Email de confirmation sous 24h
-
Si CV retenu, un recruteur vous contacte pour un call
-
Échange de 15–30 min pour valider l’adéquation profil/poste
-
Entretien virtuel avec le manager recruteur
-
Entretiens virtuels ou en présentiel avec d’autres intervenants
-
GE HealthCare en images


La carte
283 Rue de la Minière
78530 Buc
Publiée le 24/04/2026 - Réf : GEVGHLGLOBALR4039690EXTERNALENGLOBAL